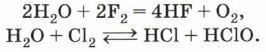|
|
|
|
|
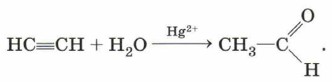
Глава вторая. Химические реакции § 17. Роль воды в химических реакциях (окончание)Взаимодействие ацетилена с водой было известно до М. Г. Кучерова. Однако практического применения эта реакция не находила из-за очень малого выхода продукта — уксусного альдегида. Заслуга русского учёного состояла в том, что он нашёл катализатор этого процесса — соли ртути, кардинально увеличившие выход продукта:
В неорганической химии реакции с участием воды также широко известны. Так, с водой при обычных условиях энергично реагируют щелочные и щёлочноземельные металлы, при этом образуются щёлочь и водород: 2Na + 2Н2O = 2NaOH + Н2↑,
Химические антиподы щелочных металлов — галогены — по-разному взаимодействуют с водой. Вода горит во фторе, а хлор, например, взаимодействует с водой достаточно медленно и обратимо:
Именно хлорноватистая кислота НСlO, один из продуктов последней реакции, определяет отбеливающее действие хлора. С основными и кислотными оксидами вода реагирует с образованием соответствующих гидроксидов — щелочей и растворимых кислот, например: ВаО + Н2O = Ва(ОН)2,
Вода участвует в процессах электролиза (разложения веществ электрическим током) и является источником получения чистых водорода и кислорода:
В свою очередь, взаимодействие водорода и кислорода служит той реакцией, которая позволяет выводить на околоземную орбиту космические корабли (см. рис. 52). Однако рассмотрением этих свойств далеко не исчерпывается роль воды как реагента. Гораздо более многочисленны и чрезвычайно важны реакции гидролиза, о которых и пойдёт речь в следующем параграфе.
1. Какое строение имеет молекула воды? Каковы её физические свойства? 2. Раскройте интегрирующую роль воды в естествознании — между химией, биологией, физикой и географией. Возможно ли без структурирования и актуализации интеграционных проблем достаточно полно сделать это? 3. Расскажите о роли воды в решении экономических проблем общества, используя возможности Интернета. 4. Раскройте глобальную проблему человечества — проблему пресной воды на Земле и предложите пути её решения на основе подготовленной презентации. 5. Расскажите о роли воды в химических реакциях. 6. Докажите, что диссоциация электролита — это результат процесса гидратации. Какую роль сыграли русские химики в изучении этой стороны теории электролитической диссоциации? 7. Что такое степень электролитической диссоциации? На какие группы делят электролиты по степени электролитической диссоциации? Приведите примеры представителей каждой группы. 8. Перечислите химические свойства воды. Какие из этих свойств находят практическое применение? 9. Что такое кристаллогидраты? Какой процесс лежит в основе наложения гипсовых повязок или изготовления изделий из алебастра? 10. Запишите уравнения реакций, с помощью которых можно осуществить следующие превращения: а) O2 → Н2O → Н2 → NH3 → Н2O → Н3РO4 → Н22O → NaOH; б) С2Н4 → С2Н5ОН → С2Н4 → СН3СНО → СН3СООН → Н2O.
|
|
|