|
|
|
|
|
Глава 6. Основные классы неорганических соединений § 31. Основания — гидроксиды основных оксидов
Приступаем к знакомству со следующим классом неорганических соединений — основаниями.
Изменение окраски фенолфталеина на малиновую свидетельствует об образовании растворимого основания Ва(ОН)2 и малорастворимого основания Са(ОН)2:
Остальные оксиды не растворились, но им также соответствуют гидроксиды — нерастворимые основания, которые получают из соединений металлов иными способами. В состав оснований всегда входят один атом металла и связанные с ним гидроксогруппы — ОН. Валентность гидроксогруппы равна единице.
Очень важно отличать растворимые основания от нерастворимых. Для этого следует запомнить, что растворимые основания, или щёлочи, образуют элементы-металлы главной подгруппы первой группы (А-группы) периодической системы, а также элементы главной подгруппы второй группы (В-группы): кальций, барий и стронций. Свойства растворимых и нерастворимых оснований существенно различаются. Для определения растворимости оснований пользуются таблицей растворимости (см. форзац книги). Основание гидроксид кальция заслуживает особого внимания. В таблице растворимости оно обозначено как малорастворимое (м). К малорастворимым относятся вещества, которые растворяются ограниченно — менее 1 г в 100 г воды. Это означает следующее: если в стакан, содержащий 100 г растворителя, поместить 10 г кристаллического гидроксида кальция, то 1 г вещества растворится, а остальные 9 г — нет. Прозрачная жидкость над осадком будет представлять собой раствор щёлочи — гидроксида кальция Са(ОН)2. Вам будет значительно удобнее составлять названия оснований, если вы воспользуетесь предложенным алгоритмом.
Щёлочи известны с давних времён. Поэтому для них характерны и исторически сложившиеся названия. Запомните их: КОН — едкое кали, NaOH — едкий натр, Са(ОН)2 — гашёная известь. Растворы гидроксидов бария и кальция также имеют исторические названия: Ва(ОН)2 — баритовая вода, Са(ОН)2 — известковая вода.
Выводы
1. Основаниями называются сложные вещества, в состав которых входят атомы металлов и гидроксогруппы. Число гидрок- согрупп определяется валентностью металла.
2. По характеру свойств различают растворимые основания (щёлочи) и нерастворимые основания. Следует запомнить щёлочи: NaOH, КОН, Ва(ОН)2, Са(ОН)2 (малорастворим).
Основные понятия
Растворимые основания — щёлочи • Нерастворимые основания • Гидроксогруппы
Вопросы и задания
1) КОН, К2O4, К2O
3) H2SO4, LiOH, Li2CO3
В выбранном ряду подчеркните щёлочи.
a) Li → Li2O → LiOH; б) Са → СаО → Са(ОН)2.
|
|
|



 Какие сведения содержит таблица растворимости? Как ею пользоваться? Какие вещества называются индикаторами? Какие индикаторы вам известны?
Какие сведения содержит таблица растворимости? Как ею пользоваться? Какие вещества называются индикаторами? Какие индикаторы вам известны?
 В четыре пробирки поместите очень маленькие порции (столько, сколько уместилось бы на кончике ножа) оксидов алюминия, бария, кальция и меди (II) и прилейте к ним по 2-3 мл воды. Взболтайте вещества в пробирках. Что произошло? Во все пробирки добавьте по нескольку капель фенолфталеина. Полученные результаты наблюдений представим в таблице 18.
В четыре пробирки поместите очень маленькие порции (столько, сколько уместилось бы на кончике ножа) оксидов алюминия, бария, кальция и меди (II) и прилейте к ним по 2-3 мл воды. Взболтайте вещества в пробирках. Что произошло? Во все пробирки добавьте по нескольку капель фенолфталеина. Полученные результаты наблюдений представим в таблице 18.

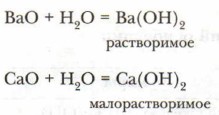


 1. Формулы только оснований приведены в ряду
1. Формулы только оснований приведены в ряду
 3. По предложенной схеме составьте соответствующие уравнения реакций:
3. По предложенной схеме составьте соответствующие уравнения реакций:
 4. Предложите объяснение следующему факту7. Название гидроксида натрия восходит к названию знаменитого в древности египетского озера Вади Натрум. Какая связь может быть прослежена между ними?
4. Предложите объяснение следующему факту7. Название гидроксида натрия восходит к названию знаменитого в древности египетского озера Вади Натрум. Какая связь может быть прослежена между ними?