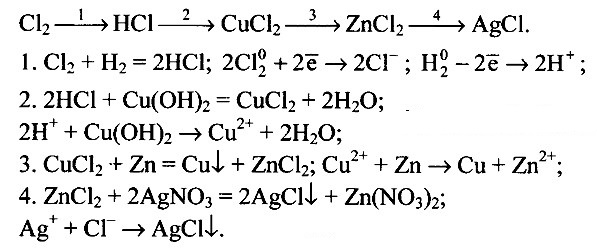|
|
|
|
|
Глава 3. Неметаллы Соединения галогенов. ОтветыОтвет на вопрос 1Электролитическая диссоциация увеличивается от HF к HI. Самая сильная из галогеноводородных кислот— иодоводородная, а самая слабая — фтороводородная. Большая прочность химической связи Н—F (фтороводородная кислота слабо диссоциирует в воде) обусловлена малым размером атома F и соответствующим малым расстоянием между ядрами атомов водорода и фтора. С ростом радиуса атома от F к I растет и межъядерное расстояние, прочность молекул уменьшается и соответствующая способность к электролитической диссоциации увеличивается. Ответ на вопрос 2
Ответ на вопрос 3
Ответ на вопрос 4
|
|
|