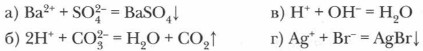|
|
|
|
|
Глава 2. Растворы. Теория электролитической диссоциации Реакции электролитов в водных растворах и их уравненияПроблема. В каких случаях обменные реакции протекают необратимо, т. е. до конца? Это имеет место в трех случаях, когда в качестве продуктов реакции ионного обмена образуются вещества, покидающие сферу реакции: а) нерастворимые вещества, выпадающие в осадок:
б) газообразные вещества, также покидающие зону реакции:
в) малодиссоциированные вещества (слабые электролиты, например вода):
Для решения вопроса о возможности протекания той или иной обменной реакции часто приходится обращаться к таблице растворимости неорганических соединений. Также необходимо помнить наиболее распространенные случаи образования газообразных соединений (углекислого и сернистого газов, аммиака). Они выделяются, если в результате реакции обмена образуются соответствующие кислоты (угольная Н2СO3 и сернистая Н2SO3 — неустойчивые, разлагающиеся в момент образования).
а) хлорида железа (III) и гидроксида натрия;
Проделайте соответствующие опыты. Запишите уравнения реакций в молекулярной и ионной форме и укажите признаки их протекания. Основные понятия Полные и сокращенные ионные уравнения • Реакции ионного обмена Вопросы и задания
|
|
|



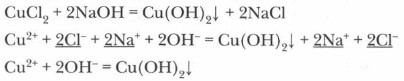
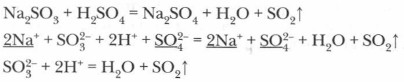
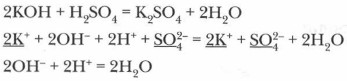
 Лабораторный опыт. Составьте прогноз относительно возможности протекания реакций ионного обмена между следующими растворами:
Лабораторный опыт. Составьте прогноз относительно возможности протекания реакций ионного обмена между следующими растворами:
 1. Какое из перечисленных веществ вступит в реакцию с раствором соляной кислоты: гидроксид бария, нитрат серебра, сульфат меди (II), нитрат натрия, сульфит калия, гидроксид аммония, оксид меди (II), оксид фосфора (V)? Составьте соответствующие уравнения реакций в молекулярной и полной ионной формах.
1. Какое из перечисленных веществ вступит в реакцию с раствором соляной кислоты: гидроксид бария, нитрат серебра, сульфат меди (II), нитрат натрия, сульфит калия, гидроксид аммония, оксид меди (II), оксид фосфора (V)? Составьте соответствующие уравнения реакций в молекулярной и полной ионной формах.
 2. Приведите не менее трех примеров химических реакций, сущность которых может быть выражена следующими сокращенными ионными уравнениями:
2. Приведите не менее трех примеров химических реакций, сущность которых может быть выражена следующими сокращенными ионными уравнениями: