|
|
|
|
|
§ 42. Первый закон термодинамики Первый закон термодинамики (продолжение)Важным достоинством формулы (6) является то, что в неё не входят ни количество вещества в газе, ни его масса. Поэтому, например, если давление и объём газа остались неизменными, то не изменилась и внутренняя энергия газа, хотя при этом могла измениться его масса. Рассмотрим пример, в котором речь идёт о воздухе, который состоит в основном из двухатомных молекул. Их средняя кинетическая энергия при заданной температуре больше, чем у одноатомных молекул (двухатомные молекулы обладают ещё кинетической энергией вращательного движения). Однако для выполнения следующего задания то, что воздух состоит из двухатомных молекул, несущественно.
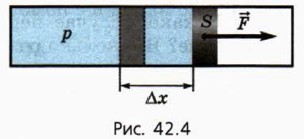
а) На сколько процентов увеличилась средняя кинетическая энергия молекул в воздухе? б) Как изменилась внутренняя энергия воздуха в комнате? в) На сколько процентов изменилась концентрация молекул воздуха? г) Насколько изменилась масса воздуха в комнате? Как найти совершённую газом работу?Рассмотрим сначала изобарное расширение газа в цилиндре под поршнем (рис. 42.4). Газ давит на поршень с силой F = pS, где р — давление газа, S — площадь поршня.
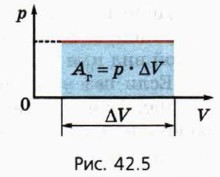
Если поршень переместился на Ах, то совершённая газом работа Δr = F • Δх = pS • Δх. Так как S • Δх = ΔV, получаем, что при изобарном расширении работа газа выражается формулой Аr = р • AV. 10 (8)
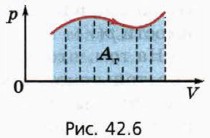
Это свойство графика зависимости p(V) сохраняется и тогда, когда давление газа изменяется. Пусть, например, график зависимости p(V) имеет вид, изображённый на рисунке 42.6. Процесс расширения газа мысленно разобьём на большое число этапов, в каждом из которых объём газа изменяется настолько мало, что его давление можно считать практически постоянным. Поскольку для каждого этапа работа газа численно равна площади под соответствующим участком графика, то и вся работа, совершённая газом при расширении, равна площади под всем графиком р(V).
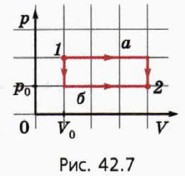
а) В каком случае совершённая газом работа больше? Во сколько раз больше? б) В каком случае изменение внутренней энергии газа больше? Во сколько раз больше? в) В каком случае переданное газу количество теплоты больше? Во сколько раз больше? На примере этого задания вы могли заметить, что изменение ΔU внутренней энергии данной массы идеального газа определяется только начальным и конечным состоянием газа.
|
|
|



 9. До включения отопления температура воздуха в комнате объёмом 60 м3 была равна 15 °С. После включения отопления воздух нагрелся до 20 °С. Давление воздуха постоянно и равно 105 Па.
9. До включения отопления температура воздуха в комнате объёмом 60 м3 была равна 15 °С. После включения отопления воздух нагрелся до 20 °С. Давление воздуха постоянно и равно 105 Па.