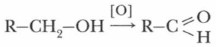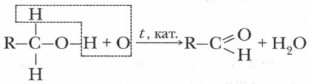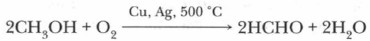|
|
|
|
|
Глава 8. Альдегиды и кетоны Применение и получение альдегидов
Применение альдегидовНаибольшее применение из альдегидов имеют формальдегид и ацетальдегид. Применение веществ основано на их свойствах. Задание. Предложите возможные способы получения формальдегида и ацетальдегида и дайте им обоснование. Формальдегид имеет широкое применение в быту. Водный раствор формальдегида называется формалином. Он используется для дезинфекции помещений, морских судов, складов, хирургических инструментов, для хранения анатомических препаратов. В сельском хозяйстве его применяют для протравливания семян. Формальдегид широко применяется и в кожевенной промышленности как дубильное вещество, делающее кожи более твердыми. Большое количество формальдегида используется в производстве пластмасс — фенолоформальдегидных, получаемых реакцией поликонденсации, и полиформальдегидных, являющихся продуктом реакции полимеризации. Фенолформальдегидные пластмассы широко применяют в электротехнике (выключатели, розетки и др.). На основе фенолформальдегидных смол готовят клеи, лаки, эмали, краски, политуры. Из полиформальдегида изготавливают литые и пленочные изделия. Ацетальдегид (уксусный альдегид) используется для производства уксусного ангидрида пластмасс, а также для других органических синтезов. Ацетальдегид и его производные идут на изготовление некоторых лекарств. В предыдущем параграфе рассматривалась реакция хлорирования уксусного альдегида, конечным продуктом которой является хлораль (трихлоруксусный альдегид). Хлораль (Сl3С—СОН) входит в состав некоторых анальгетиков (обезболивающих средств). Но в основном его применение связано с получением инсектицидов (средств для борьбы с несекомыми) и хлороформа — анестезирующего вещества. При растворении хлораля в воде образуется хлоральгидрат ССl3СН(ОН)2. Получение альдегидовОбщим способом получения всех альдегидов является окисление спиртов. Уравнение реакции в общем виде:
С примерами окисления спиртов в альдегиды вы встречались при изучении темы «Спирты». Задание. Вспомните лабораторный опыт окисления этилового спирта с помощью медной проволоки. Запишите уравнение этой реакции. Рассмотрим ее схему:
В промышленных условиях метаналь, или формальдегид, получают, пропуская через реактор смесь паров метанола с воздухом над поверхностью раскаленной медной или серебряной сетки (катализатора).
|
|
|



 Изучая химические реакции углеводородов и спиртов, вы уже встречались с некоторыми способами получения альдегидов. Вспомните их и запишите ураовнения химических реакций.
Изучая химические реакции углеводородов и спиртов, вы уже встречались с некоторыми способами получения альдегидов. Вспомните их и запишите ураовнения химических реакций.