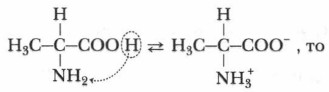|
|
|
|
|
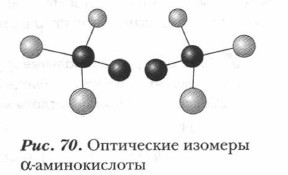
Глава 13. Аминокислоты. Пептиды. Белки Аминокислоты. Состав, строение, свойстваОптическая изомерия аминокислотα-Аминокислоты могут существовать в двух формах, которые отличаются друг от друга взаимным расположением заместителей. Они отличаются друг от друга, как левая и правая перчатки, как любой предмет от своего зеркального отражения (рис. 70).
Два типа оптических изомеров отличаются и по некоторым свойствам. Так, они обладают способностью вращать луч поляризованного света в разных направлениях. Те молекулы, которые вращают его вправо, относятся к D-ряду (от лат. dexter — «правый»). А другие, вращающие луч поляризованного света влево, именуются левовращающими и относятся к L-ряду (от лат. laevus — «левый»).
Физические свойства аминокислотАминокислоты, как правило, являются растворимыми в воде, бесцветными кристаллическими веществами. Многие имеют сладкий вкус. Задание. Как, исходя из особенностей строения аминокислот, объяснить их растворимость в воде? Химические свойства аминокислотПроблема. Учитывая особенности состава и строения аминокислот, попытайтесь охарактеризовать их кислотно-основные свойства. Как вы полагаете, какое действие аминокислоты оказывают на индикаторы, например на лакмус? Гетерофункционалъная природа аминокислот проявляется в том, что наличие карбоксильной группы, обеспечивающей кислотные свойства, и аминогруппы, придающей соединению основные свойства, определяет амфотерный характер их химических свойств. Если в растворе устанавливается равновесие между ионной и молекулярной формами
раствор аминокислоты имеет нейтральный характер. При этом действие на индикатор одной функциональной группы нейтрализуется противоположным действием второй группы. Отщепление протона от карбоксильной группы при диссоциации аминокислоты и присоединение протона аминогруппой приводит к образованию биполярного иона (цвиттер-иона).
|
|
|



 D- и L-формы кислот способны постепенно, довольно медленно превращаться друг в друга. В живых тканях левовращающие формы постепенно превращаются в правовращающие. Так, например, в белке костной ткани зубов 0,1 % L-аспарагиновой кислоты за год преобразуется в D-форму. Поэтому по содержанию правовращающей формы в ткани зуба можно определить возраст всего организма. Это стало основанием для разработки особого метода определения возраста как живых тканей, так и ископаемых остатков животных.
D- и L-формы кислот способны постепенно, довольно медленно превращаться друг в друга. В живых тканях левовращающие формы постепенно превращаются в правовращающие. Так, например, в белке костной ткани зубов 0,1 % L-аспарагиновой кислоты за год преобразуется в D-форму. Поэтому по содержанию правовращающей формы в ткани зуба можно определить возраст всего организма. Это стало основанием для разработки особого метода определения возраста как живых тканей, так и ископаемых остатков животных.