|
|
|
|
|
Глава 13. Аминокислоты. Пептиды. Белки § 46. Аминокислоты. Состав, строение, свойства (окончание)Добавлением сильной кислоты можно превратить аминокислоту в катион:
Добавление к раствору сильного основания также приводит к ионизации:
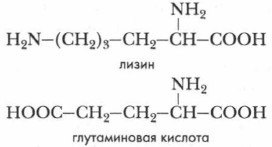
Это свойство образовывать нейтральные растворы не характерно для тех аминокислот, в молекулах которых содержится неодинаковое число карбоксильных и аминогрупп. Например:
Действие таких аминокислот на индикатор зависит от преобладания в их составе карбоксильных или аминогрупп.
Двойственность химических функций аминокислот, в частности, проявляется в их способности взаимодействовать с кислотами и с основаниями, т. е. к амфотерности. Проявляя кислотные свойства, они вступают в реакции со щелочами с образованием солей:
Проявляя осно́вные свойства, реагируют с кислотами, образуя соли: NH2—CH2—CH2—COOH + НСl → [H3N—CH2—CH2—COOH]+Cl- Со спиртами взаимодействуют с образованием сложных эфиров:
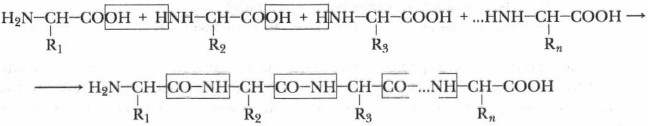
Очень важным свойством аминокислот является их способность вступать друг с другом в реакцию конденсации:
Чтобы научиться составлять такие уравнения, важно запомнить, что формулы аминокислот имеют единый план записи: слева записывается аминогруппа, справа — карбоксил. Группа атомов —СО—NH—, образующаяся при взаимодействии молекул аминокислот, называется пептидной, или амидной, группой, а связь между атомами углерода и азота в ней — пептидной (амидной) связью. Соединение, образовавшееся при взаимодействии двух аминокислот, называется дипептидом. Поскольку каждая аминокислота обладает по крайней мере двумя функциональными группами, то возможно дальнейшее присоединение к дипептиду новых молекул аминокислот. В результате образования каждой новой пептидной (амидной) связи выделяется молекула воды. В результате этой реакции синтезируются молекулы пептидов и полипептидов с большим числом аминокислотных звеньев. Белок представляет собой полипептид, содержащий сотни или тысячи аминокислотных звеньев. Основные понятия α-Аминокислоты. Оптические изомеры: L-ряд и D-ряд. Гетерофункциональная природа, амфотерность. Пептидная (амидная) связь, дипептид, полипептид Вопросы и задания
|
|
|



 Если обе функциональные группы ионизированы в равной степени, об аминокислоте говорят, что она находится в изоэлектрической точке.
Если обе функциональные группы ионизированы в равной степени, об аминокислоте говорят, что она находится в изоэлектрической точке.
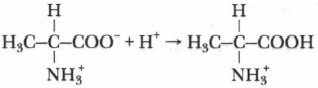
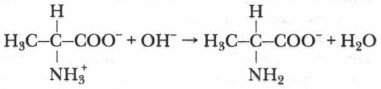
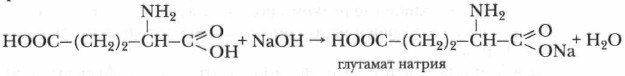
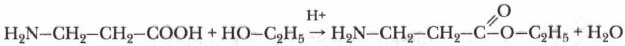
 1. По признаку наличия в аминокислоте амино- и карбоксильных групп их подразделяют на нейтральные, осно́вные и кислотные. Приведите примеры для каждой из групп кислот.
1. По признаку наличия в аминокислоте амино- и карбоксильных групп их подразделяют на нейтральные, осно́вные и кислотные. Приведите примеры для каждой из групп кислот.
 2. Пользуясь формулами аминокислот, приведенными в таблице 20, составьте уравнение реакции получения любого трипептида.
2. Пользуясь формулами аминокислот, приведенными в таблице 20, составьте уравнение реакции получения любого трипептида.