|
|
|
|
|
Глава 6. Спирты, фенолы Фенолы3. Вы наблюдали реакцию фенола с бромной водой. Признаком её было образование белого осадка трибромфенола, его формула С6Н2Вr3—ОН, которая доказана экспериментально (см. структурную формулу на с. 139). Три атома водорода в бензольном кольце замещаются на атомы брома. Задание. Запишите уравнение реакции брома с бензолом. Бензол с бромной водой не реагирует, а с бромом взаимодействует лишь при наличии катализатора (железные опилки), причём бром замещает в бензольном ядре только один атом водорода. Проблема. Реакция брома с фенолом протекает с большей лёгкостью, чем с бензолом, и при этом замещаются в бензольном кольце три атома водорода, а не один, как у бензола. Почему? Постарайтесь решить эту проблему самостоятельно!
На примере фенола вы наглядно убедились в реальности учения о взаимном влиянии атомов в молекулах, разработанного А.М. Бутлеровым и его учеником В.В. Марковниковым.
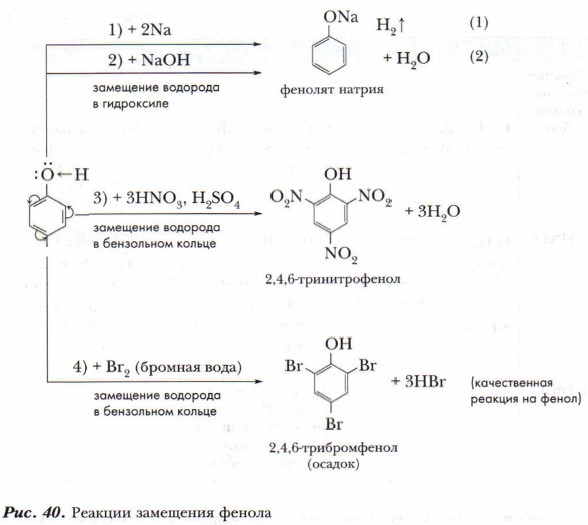
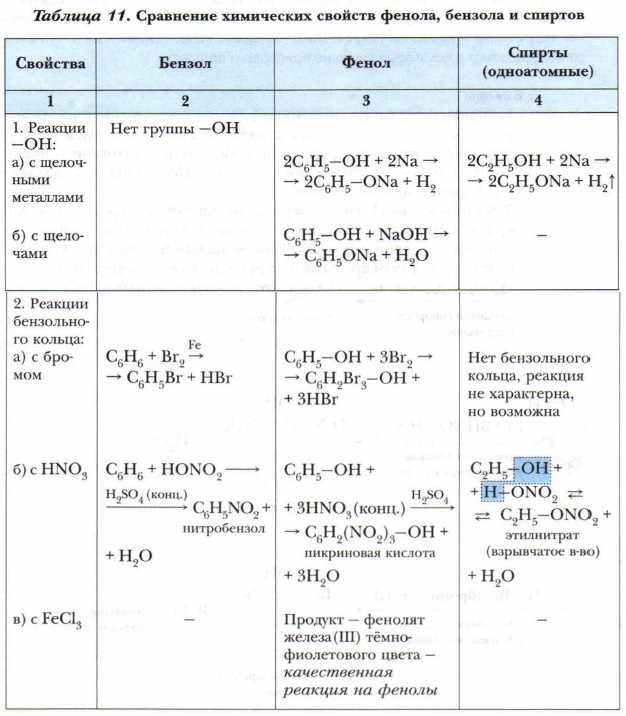
Итак, для фенола характерны реакции замещения (рис. 40). Обобщим наши наблюдения и знания о химических свойствах фенола в таблице 11. Получение и применение феноловФенолы выделяют из каменноугольной смолы, из продуктов переработки бурого угля, торфа и древесины. Их получают синтезом из бензола и его производных, которые образуются при крекинге нефти. Фенол чрезвычайно опасен для животных и растений. Поэтому при производстве и использовании фенола особое внимание уделяют экологическим проблемам, связанным с защитой природы от промышленных отходов, содержащих фенол. Фенол в больших количествах применяется для производства красителей, фенолформальдегидных пластмасс, лекарственных веществ. В медицине для дезинфекции помещений и мебели применяют лизол, в состав которого входят разные фенолы.
Некоторые неопасные для человека фенолы и их производные используют как антиоксиданты — вещества, предотвращающие порчу пищевых продуктов при их долгом или неправильном хранении (жиров, масел, пищевых концентратов и др.). Антиоксиданты добавляют в некоторые пищевые приправы и продукты.
Выводы 1. Фенолы — производные ароматических углеводородов (прежде всего бензола), в молекулах которых одна или несколько гидроксильных групп непосредственно соединены с атомами углерода ароматического (бензольного) кольца. Простейший и важнейший представитель — фенол. 2. Фенол ядовит! Это — твёрдое, бесцветное, гигроскопическое кристаллическое вещество с резким запахом. Его химические свойства обусловлены как функциональной группой —ОН, так и углеводородным ароматическим радикалом — фенилом (C6H5—). На свойствах фенола сказывается взаимное влияние гидроксильной группы и бензольного ядра: в отличие от спиртов он способен взаимодействовать как слабая кислота со щелочами, а в отличие от бензола в реакциях замещения атомов водорода бензольного кольца фенол образует 2,4,6-производные (трибромфенол, тринитрофенол и др.). 3. Фенолы находят широкое применение в медицине как антисептические и дезинфицирующие средства, в пищевой промышленности как антиоксиданты, в химическом производстве как сырьё для производства пластмасс, лекарств и других продуктов. Основные понятия Фенолы • Радикал фенил • Строение молекулы фенола • Взаимное влияние радикала и функциональной группы • Особенности проявления химических свойств • Антиоксиданты • Качественная реакция на фенол Вопросы и задания
а) с натрием
|
|
|



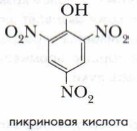
 4. В реакцию с фенолом могут вступать не только галогены. Аналогично и с большой лёгкостью протекает реакция фенола с азотной кислотой, где основным продуктом является 2,4,6-тринитрофенол, называемый пикриновой кислотой, которая служит основой производства взрывчатых веществ и красителей.
4. В реакцию с фенолом могут вступать не только галогены. Аналогично и с большой лёгкостью протекает реакция фенола с азотной кислотой, где основным продуктом является 2,4,6-тринитрофенол, называемый пикриновой кислотой, которая служит основой производства взрывчатых веществ и красителей.
 1. Какие соединения называются фенолами и в чём их отличие от ароматических спиртов?
1. Какие соединения называются фенолами и в чём их отличие от ароматических спиртов?
 2. Напишите структурную формулу фенола и объясните причину смещения электронной плотности в молекуле.
2. Напишите структурную формулу фенола и объясните причину смещения электронной плотности в молекуле.
 3. Чем обусловлены кислотные свойства фенола и почему они выражены сильнее, чем у спиртов? Докажите ваше мнение.
3. Чем обусловлены кислотные свойства фенола и почему они выражены сильнее, чем у спиртов? Докажите ваше мнение.
 6. Используя дополнительную литературу и другие источники информации (Интернет), составьте сообщение о воздействии фенола и его производных на окружающую среду.
6. Используя дополнительную литературу и другие источники информации (Интернет), составьте сообщение о воздействии фенола и его производных на окружающую среду.