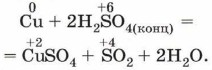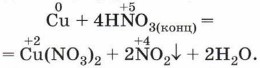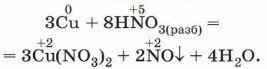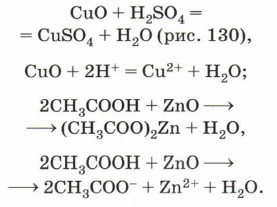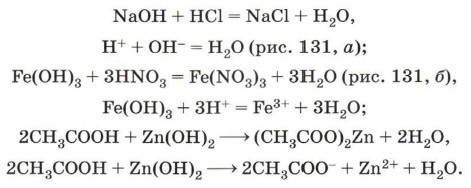|
|
|
|
|
Глава третья. Вещества и их свойства § 22. Кислоты (продолжение)Взаимодействие кислот с металламиЭто свойство уже было подробно рассмотрено в § 20 (см. с. 167—168).
Рассмотрим особенности взаимодействия с металлами азотной кислоты и концентрированной серной кислоты. Эти кислоты взаимодействуют с металлами, стоящими в электрохимическом ряду напряжений как до, так и после водорода, не образуя при этом водород. В результате реакций этих кислот с металлами образуются соль, вода и продукт восстановления сульфат- или нитратанионов. Так, при взаимодействии концентрированной серной кислоты с медью образуется оксид серы (IV):
При взаимодействии концентрированной азотной кислоты с медью образуется бурый оксид азота (IV) (рис. 128):
В реакции меди с разбавленной азотной кислотой в качестве продукта восстановления нитрат-иона образуется бесцветный оксид азота (II):
Концентрированная серная кислота обугливает органические вещества (рис. 129), так как очень гигроскопична (вспомните правило разбавления серной кислоты). Взаимодействие кислот с оксидами металлов
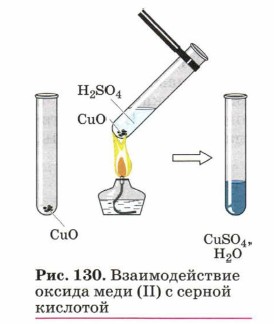
С осно́вными и амфотерными оксидами взаимодействуют как неорганические, так и органические оксиды. Например:
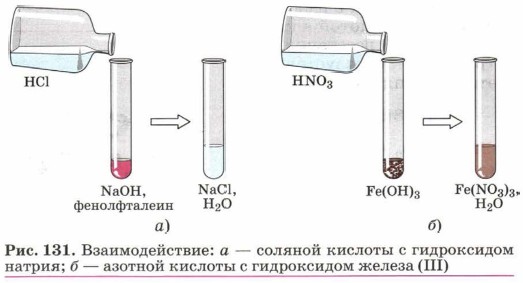
Взаимодействие кислот с гидроксидами металловС основаниями (с щелочами и нерастворимыми в воде основаниями) и амфотерными гидроксидами также взаимодействуют как органические, так и неорганические кислоты.
|
|
|