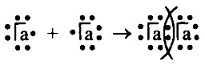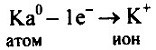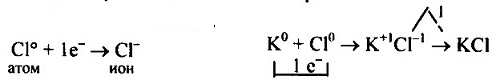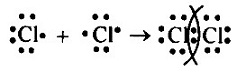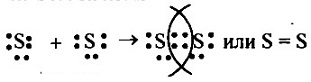|
|
|
|
|
Глава первая. Атомы химических элементов Взаимодействие атомов элементов-неметаллов между собой. ОтветыОтвет на вопрос 1Электронная схема образования двухатомной молекулы галогена будет выглядеть так:
А структурная формула: Hal — Hal Ответ на вопрос 2а) Схема образования химической связи для КСl: Калий — элемент 1 группы, его атому легче отдать 1 внешний электрон, чем принять недостающие 7.
Хлор — элемент VII группы, его атому легче принять 1 недостающий электрон, чем отдать 7 электронов.
б) Схема образования химической связи для Сl2: Хлор - элемент главной подгруппы VII группы. Его атомы имеют 7 электронов на внешнем уровне. Число непарных электронов равно (8-7) 1.
Связь между атомами одного и того же элемента ковалентна. Ответ на вопрос 3Сера— элемент главной подгруппы VI группы. Ее атомы имеют 6 электронов на внешнем уровне. Число непарных электронов равно (8-6)2. В молекулах S2 атомы связаны двумя общими электронными парами, поэтому связь двойная. Mega resheba. VTI Схема образования молекулы S2 будет выглядеть следующим образом:
Ответ на вопрос 4В молекуле S2 связь двойная, в молекуле Сl связь одинарная, в молекуле N2 — тройная. Поэтому самой прочной модекулой будет N2, менее прочной S2, а еще слабее Cl2. Длина связи самая маленькая в молекуле N2, больше в молекуле S2, еще больше в молекуле Сl2. Ответ на вопрос 5Вещества с ковалентной неполярной связью: N2, O2, Н2. Вещества с ионной связью: Li2O,KСl, CaF2.
|
|
|