|
|
|
|
|
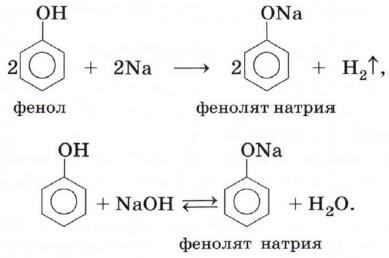
Глава 4. Кислородсодержащие соединения ФенолыХимические свойства фенолаКислотные свойстваКак уже было сказано, атом водорода гидроксильной группы фенола обладает кислотным характером. Кислотные свойства у фенола выражены сильнее, чем у воды и спиртов. В отличие от спиртов и воды фенол реагирует не только с щелочными металлами, но и с щелочами с образованием фенолятов:
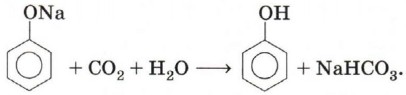
Однако кислотные свойства у фенолов выражены слабее, чем у неорганических и карбоновых кислот. Так, например, кислотные свойства фенола примерно в 3000 раз слабее, чем у угольной кислоты. Поэтому, пропуская через водный раствор фенолята натрия углекислый газ, можно выделить свободный фенол:
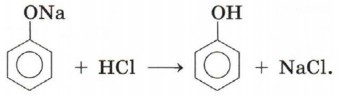
Добавление к водному раствору фенолята натрия соляной или серной кислоты также приводит к образованию фенола:
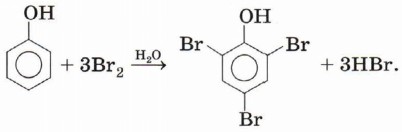
Качественная реакция на фенолФенол реагирует с хлоридом железа (III) с образованием окрашенного в фиолетовый цвет комплексного соединения. Эта реакция позволяет обнаруживать его даже в очень незначительных количествах. Другие фенолы, содержащие одну или несколько гидроксильных групп в бензольном кольце, также дают яркое окрашивание от сине-фиолетовых до красно-коричневых оттенков в реакции с хлоридом железа (III). Реакции бензольного кольцаНаличие гидроксильного заместителя значительно облегчает протекание реакций электрофильного замещения в бензольном кольце. Бромирование фенола. В отличие от бензола, для бромирования фенола не требуется добавления катализатора. Кроме того, взаимодействие с фенолом протекает селективно (избирательно): атомы брома направляются в орто- и пара-положения, замещая находящиеся там атомы водорода. Селективность замещения объясняется рассмотренными выше особенностями электронного строения молекулы фенола. Так, при взаимодействии фенола с бромной водой образуется белый осадок 2,4,6-трибромфенола:
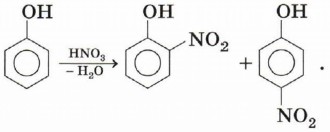
Эта реакция, как и реакция с хлоридом железа (III), служит для обнаружения фенола. Нитрование фенола. Реакция также происходит легче, чем нитрование бензола. С разбавленной азотной кислотой она идёт при комнатной температуре. В результате образуется смесь орто- и пара-изомеров нитрофенола:
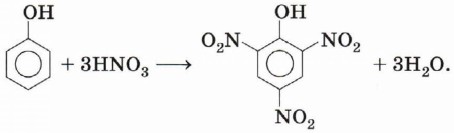
При использовании концентрированной азотной кислоты образуется 2,4,6-тринитрофенол — пикриновая кислота, взрывчатое вещество:
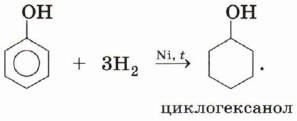
Гидрирование ароматического ядра фенола. В присутствии катализатора реакция происходит легко:
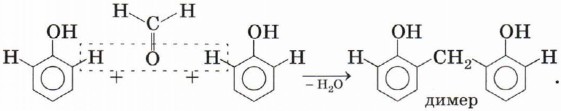
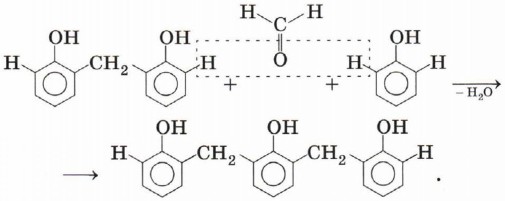
Поликонденсация фенола с альдегидами. С формальдегидом реакция происходит с образованием продуктов — фенолоформальдегидных смол и твёрдых полимеров. Взаимодействие фенола с формальдегидом можно описать схемой:
Вы, наверное, заметили, что в молекуле димера сохраняются «подвижные» атомы водорода, а значит, при достаточном количестве реагентов возможно продолжение реакции:
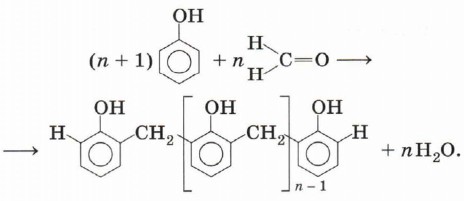
Реакция поликонденсации — получения полимера, протекающая с выделением побочного низкомолекулярного продукта (например, воды, аммиака и др.) может продолжаться и далее (до полного израсходования одного из реагентов) с образованием огромных макромолекул. Процесс можно описать суммарным уравнением
Образование линейных молекул происходит при обычной температуре. При нагревании образующийся продукт приобретает разветвлённое строение. Он твёрдый и нерастворимый в воде. В результате нагревания фенолоформальдегидной смолы линейного строения с избытком альдегида получаются твёрдые пластические массы с уникальными свойствами. Фенол и продукты на его основе находят широкое применение (рис. 44). Полимеры на основе фенолоформальдегидных смол применяют для изготовления лаков и красок. Пластмассовые изделия, изготовленные на основе этих смол, устойчивы к нагреванию, охлаждению, действию воды, щелочей и кислот, также они обладают высокими диэлектрическими свойствами. Из полимеров на основе фенолоформальдегидных смол изготавливают детали электроприборов, корпуса силовых агрегатов и детали машин, полимерную основу печатных плат для радиоприборов. Клеи на основе фенолоформальдегидных смол способны надёжно соединять детали самой различной природы, сохраняя высочайшую прочность соединения в очень широком диапазоне температур. Такой клей применяется для крепления металлического цоколя ламп освещения к стеклянной колбе. Теперь вам стало понятно почему.
|
|
|