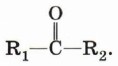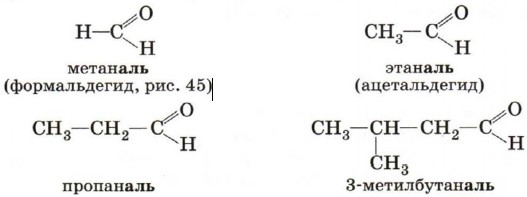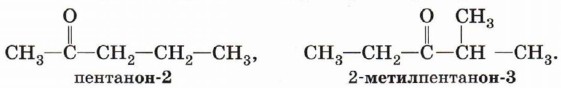|
|
|
|
|
Глава 4. Кислородсодержащие соединения § 19. Альдегиды и кетоныСтроение альдегидов и кетонов
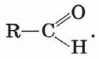
Общая формула альдегидов имеет вид
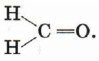
В простейшем альдегиде — формальдегиде — роль углеводородного радикала играет атом водорода:
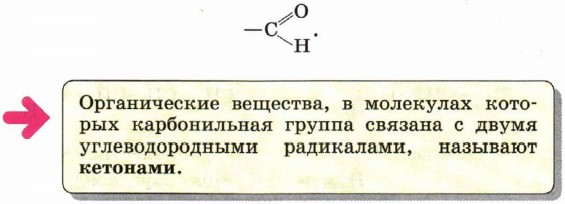
Карбонильную группу, связанную с атомом водорода, часто называют альдегидной:
Общая формула кетонов имеет вид
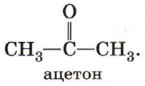
Карбонильную группу кетонов называют кетогруппой. В простейшем кетоне — ацетоне — карбонильная группа связана с двумя метильными радикалами:
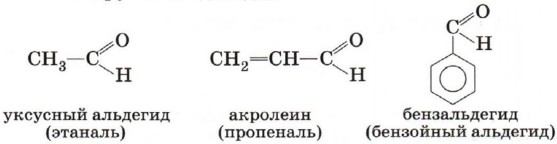
Номенклатура и изомерияВ зависимости от строения углеводородного радикала, связанного с альдегидной группой, различают предельные, непредельные, ароматические, гетероциклические и другие альдегиды.
В соответствии с номенклатурой ИЮПАК названия предельных альдегидов образуются от названия алкана с тем же числом атомов углерода в молекуле с помощью суффикса -аль. Например:
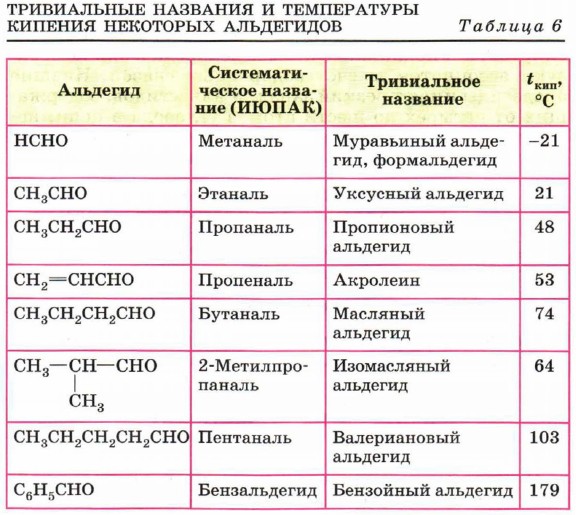
Нумерацию атомов углерода главной цепи начинают с атома углерода альдегидной группы. Поскольку эта функциональная группа всегда располагается на конце углеродной цепи, альдегидный атом углерода получает номер 1 и указывать цифрой положение этой группы в названии вещества нет необходимости. Наряду с систематической номенклатурой используют и тривиальные названия широко применяемых альдегидов (табл. 6). Эти названия, как правило, образованы от названий карбоновых кислот, соответствующих альдегидам. Для названия кетонов по систематической номенклатуре кетогруппу обозначают суффиксом -он и цифрой, которая указывает номер атома углерода карбонильной группы (нумерацию следует начинать от ближайшего к кетогруппе конца цепи). Например:
Для альдегидов характерен только один вид структурной изомерии — изомерия углеродного скелета, которая возможна с бутаналя (см. табл. 6), а для кетонов
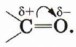
также и изомерия положения карбонильной группы (запишите структурные формулы изомеров пентанона и назовите их). Кроме этого, для них характерна и межклассовая изомерия (пропаналь и пропанон). Физические свойства альдегидов и кетоновВ молекуле альдегида или кетона вследствие большей электроотрицательности атома кислорода по сравнению с углеродным атомом связь С = 0 сильно поляризована за счёт смещения электронной плотности π-связи к кислороду:
Альдегиды и кетоны — полярные вещества с избыточной электронной плотностью на атоме кислорода. Низшие члены ряда альдегидов и кетонов (формальдегид, уксусный альдегид, ацетон) растворимы в воде неограниченно. Их температуры кипения ниже, чем у соответствующих спиртов (см. табл. 6). Это связано с тем, что в молекулах альдегидов и кетонов, в отличие от спиртов, нет подвижных атомов водорода и они не образуют ассоциатов за счёт водородных связей. Низшие альдегиды имеют резкий запах. У альдегидов, содержащих от четырёх до шести атомов углерода в цепи, неприятный запах. Высшие альдегиды и кетоны обладают цветочными запахами и применяются в парфюмерии. Химические свойства предельных альдегидов и кетоновНаличие альдегидной группы в молекуле определяет характерные свойства альдегидов.
|
|
|